



소포체 스트레스 제어를 통한 렙틴 저항성 및 비만 치료
이재민(DGIST 뉴바이올로지 전공)
최근 급증하는 비만 및 과체중 인구의 증가는 현대사회에 있어 심각한 건강 문제가 되고 있다. 미국의 경우 성인 인구의 1/3 이상이 Body Mass Index(BMI)가 30이상인 비만이고, 2/3 이상은 비만을 포함한 BMI 25이상인 과체중이다. 비만의 급증은 단순히 미국만의 문제가 아니라 우리나라를 포함한 전세계적인 문제가 되고 있다. 비만은 단순히 체중의 증가만의 문제가 아닌데, 비만 및 과체중은 최근 급증하는 제2형 당뇨병 뿐 아니라 이상지질혈증, 고혈압, 심혈관질환 등의 다양한 대사질환의 원인을 제공한다. 그리고 또한 최근 많은 연구들은 대장암이나 췌장암 등 특정 암의 발병에 비만이 부정적인 영향을 준다고 밝히고 있다.
비만 및 이로 인한 다양한 대사질환의 경우 우리 몸의 대사항상성(metabolic homeostasis) 유지에 문제가 있을때 일어난다. 체중 조절은 지방조직에서 분비되는 렙틴(Leptin, 그림 1)을 비롯해서 위에서 분비되는 Ghrelin, 장에서 분비되는 CCK(cholecystokinin) 등 다양한 호르몬 및 신경 연결을 통해 이루어 진다. 그중 대표적인 체중 조절 호르몬인 렙틴은 지방조직 세포에서 주로 합성 및 분비가 이루어 지는데, 혈액 속으로 분비된 렙틴은 궁극적으로 뇌의 시상하부(hypothalamus), 특히 arcuate nucleus에 존재하는 두가지 다른 신경세포군인 AgRP(agouti-related peptide) 및 POMC(Proopiomelanocortin) 신경세포에 작용해서 음식 섭취를 억제하고 에너지소비(energy expenditure)를 촉진함으로써 체중 감소를 유도한다. POMC 신경세포는 POMC 단백질을 만드는데, 이는 proprotein으로 세포내에서 단백질 절단효소(proprotein convertase)에 의해 α-melanocyte-stimulating hormone(αMSH, α-melanotropin)를 포함한 여러 펩티드로 바꿔준다. αMSH는 postsynaptic neuron인 MC4R(melanocortin 4 receptor) 신경세포에 존재하는 MC4R에 결합함으로써 음식섭취 행위를 억제하고 에너지소비를 증가시킨다. 이와 반대로 AgRP 신경세포는 NPY(neuropeptide Y)와 AgRP 펩티드 분비를 통해 POMC 및 MC4R 신경세포를 억제함으로써 음식섭취 행위를 유도한다. 렙틴은 렙틴 수용체와 결합해서 POMC 신경세포를 활성화하고 AgRP 신경세포의 활성을 억제한다.
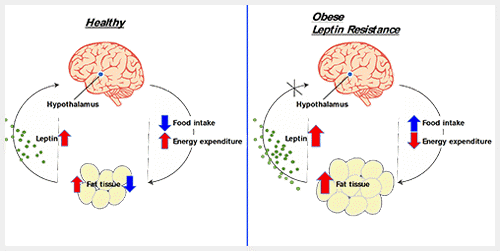
렙틴을 통한 체중 조절 항상성 기전이 존재함에도 현재 비만이 급증하는 이유는 과영양과 운동부족이 렙틴 저항성을 유도하기 때문이다(그림 1). 비만인 사람이나 동물모델에서 혈액 속 렙틴의 양은 비만이 아닌 경우보다 오히려 많은데, 렙틴이 뇌 속으로의 전달에 문제가 있거나 시상하부의 렙틴 수용체를 통한 신호전달계 활성화 저해 등을 렙틴 저항성 및 비만의 원인으로 보고있다. 항비만치료제로 GLP-1 receptor agonist, lorcaserin, phentermine, orlistat 등이 이용되고 있으나, 렙틴 저항성이 비만의 주된 원인에도 렙틴 저항성 극복을 통한 비만치료제는 나와있지 않다. 최근 진행되고 있는 연구들은 비만 및 렙틴 저항성이 시상하부 내 세포들의 세포내 스트레스(Intracellular stress), 특히 소포체 스트레스(endoplasmic reticulum stress, ER stress)에 의해 유도되고, 소포체 스트레스를 경감시키면 렙틴 저항성 극복과 함께 비만이 완화됨을 보임으로써, 소포체 스트레스 관련 신호전달계들이 비만과 같은 대사질환 치료에 이용될 수 있음을 시사하고 있다.
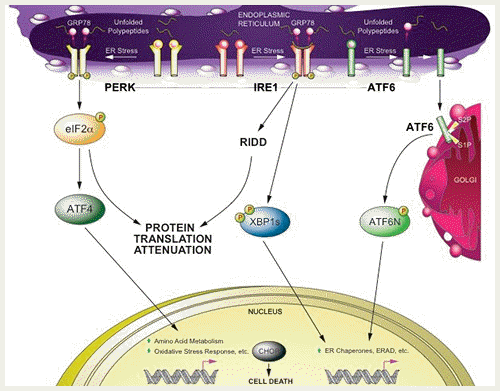
소포체 스트레스는 소포체 내에서 적절한 삼차구조 형성에 실패한(misfolded) 분비단백질이나 막단백질들이 축적됨으로써 발생한다. 소포체 스트레스가 발생하면 세포는 신호전달계를 이용해서 세포내 항상성을 유지하려고 하는데, 이를 미접힘단백질반응(unfolded protein response, 줄여서 UPR)이라고 한다 (1). 동물세포에서는 소포체에 존재하는 세종류의 막단백질들에 의해 UPR이 시작되는데, 이들은 PERK (protein kinase RNA-like ER kinase), IRE1 (inositol-requiring protein-1), ATF6 (activating transcription factor-6)이다 (그림 2). PERK은 소포체 스트레스 하에서eIF2α(eukaryotic initiation factor 2α)의 인산화를 통해 전반적인 단백질 번역(protein translation)을 억제한다. IRE1은 소포체 스트레스 하에서XBP1 mRNA를 splicing시키고, spliced XBP1(sXBP1 또는 XBP1s) mRNA는 XBP1s 전사인자를 만들어 낸다. ATF6는 소포체 스트레스 하에서 골지(the Golgi)로 이동을 해서 골지에 있는 단백질 절단 효소인 S1P(site-1 protease)와 S2P에 의해 막으로부터 전사인자 기능을 하는 도메인이 분리된다. 분리된 ATF6는 핵으로 이동해서 타겟 유전자 발현을 증가시킨다. ATF6와 XBP1s는 소포체 항상성 회복에 관여하는 유전자들의 발현을 증가시킴으로써 소포체 스트레스를 경감시키는 역할을 한다(그림 2).
소포체 스트레스 감소효과가 있다고 보고된 4-phenylbutyric acid(4-PBA)나 tauroursodeoxycholic acid(TUDCA) 같은 화합물들(이들을 chemical chaperone이라 칭함)을 렙틴 저항성을 가진 동물 모델에 처리하면 추가로 주입된 렙틴에 반응해서 비만이 완화된다. 하지만, 이들 화합물들의 항비만 효과는 제한적이어서 보다 효과적인 항비만 효과를 보이는 chemical chaperone들을 CMAP(connectivity map)을 이용해서 탐색해 보았다.
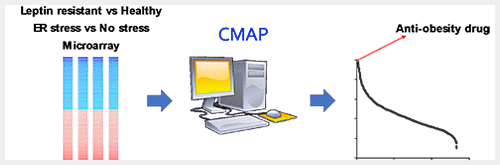
CMAP은 미국의 Broad institute (MIT와 하버드 대학이 공동으로 세운 생명과학 연구소)에서 개발한 온라인 소프트웨어로 여러 화합물들을 각각 세포에 처리한 후의 microarray 분석 정보를 저장하고 연구자들이 이용할 수 있게 되어있다. 연구자들은 자신들이 관심있는 특정 상태 하에서의 유전자 발현 양상(증가 또는 감소한 유전자 정보)을 CMAP에 넣어주면 어떤 약물들이 원하는 조건과 유사한 유전자 발현 상태를 만드는 지를 순위를 매겨서 알려준다(웹주소https://portals.broadinstitute.org/cmap/) (2). 이를 이용해서 소포체 스트레스 및 렙틴 저항성이 없는 상태에서의 유전자 발현 양상을 CMAP에 넣어서 celastrol이라는 약물이 유사한 유전자 발현을 만들어낸다는 것을 찾아내었다. Celastrol이 과연 항비만 약물로 작용하는지를 렙틴 저항성을 가지는 high-fat diet를 먹인 마우스에 처리를 했더니, 렙틴과 비슷하게 음식 섭취 억제 및 지방 조직의 감소를 통해 체중을 감소시키는 것을 관찰하였다. 기존 chemical chaperone들과 달리 celastrol은 렙틴 추가 주입없이 이미 렙틴 저항성 때문에 증가된 체내의 렙틴을 효과적으로 이용한다. 렙틴 저항성이 없는 정상 마우스와 렙틴 및 렙틴 수용체가 결실된 ob/ob나 db/db 같은 비만 마우스에게는 체중 감소 효과가 없는 것으로 봐서 celastrol은 소포체 스트레스 및 렙틴 저항성을 극복을 통해 비만을 완화시킨다는 것을 확인하였다 (3). 또한 celastrol과 비슷한 유전자 발현 양상을 보이는 다른 약물들을 CMAP을 통해서 탐색해서 withaferin A라는 약물을 찾았고, withaferin A 또한 celastrol과 비슷한 유전자 발현을 보일 뿐 아니라 celastrol 같이 소포체 스트레스 및 렙틴 저항성 극복을 통해 항비만 효과를 보이는 것을 확인하였다 (4). 이는 소포체 스트레스를 타겟하는 약물들이 렙틴 저항성 및 비만 치료에 효과적으로 이용될 수 있음을 시사한다.
비만은 현재 심각한 건강 문제로 대두되고 있으나 치료법들은 아직은 제한적이다. 소포체 스트레스 및 다른 세포내 스트레스들이 많은 질병들의 원인이 된다는 보고들은 계속 증가 중이고, 관련 기전에 대한 연구 또한 많이 진행되고있다. 이를 통해 축적된 정보들은 향후 비만과 당뇨병과 같은 대사질환을 비롯해서 세포내 스트레스에 의해 발병되는 다른 많은 질환들의 효과적인 치료법 개발에 유용하게 이용될 것으로 기대한다. 또한 CMAP과 같은 새로운 reverse pharmacology 접근법을 사용해서 유용한 약물후보군 발굴에 이용할 수 있는데, 최근 업그레이드된 CMAP이 개발되어 나와있어 신약개발에 있어 앞으로의 성과가 기대된다 (5).
1. Lee, J. and Ozcan, U. (2014) Unfolded protein response signaling and metabolic diseases. J Biol Chem 289, 1203-1211.
2. Lamb, J., Crawford, E. D., Peck, D., Modell, J. W., Blat, I. C., Wrobel, M. J., Lerner, J., Brunet, J. P., Subramanian, A., Ross, K. N., Reich, M., Hieronymus, H., Wei, G., Armstrong, S. A., Haggarty, S. J., Clemons, P. A., Wei, R., Carr, S. A., Lander, E. S. and Golub, T. R. (2006) The Connectivity Map: using gene-expression signatures to connect small molecules, genes, and disease. Science 313, 1929-1935.
3. Liu, J., Lee, J., Salazar Hernandez, M. A., Mazitschek, R. and Ozcan, U. (2015) Treatment of obesity with celastrol. Cell 161, 999-1011.
4. Lee, J., Liu, J., Feng, X., Salazar Hernandez, M. A., Mucka, P., Ibi, D., Choi, J. W. and Ozcan, U. (2016) Withaferin A is a leptin sensitizer with strong antidiabetic properties in mice. Nat Med 22, 1023-1032.
5. Subramanian, A., Narayan, R., Corsello, S. M., Peck, D. D., Natoli, T. E., Lu, X., Gould, J., Davis, J. F., Tubelli, A. A., Asiedu, J. K., Lahr, D. L., Hirschman, J. E., Liu, Z., Donahue, M., Julian, B., Khan, M., Wadden, D., Smith, I. C., Lam, D., Liberzon, A., Toder, C., Bagul, M., Orzechowski, M., Enache, O. M., Piccioni, F., Johnson, S. A., Lyons, N. J., Berger, A. H., Shamji, A. F., Brooks, A. N., Vrcic, A., Flynn, C., Rosains, J., Takeda, D. Y., Hu, R., Davison, D., Lamb, J., Ardlie, K., Hogstrom, L., Greenside, P., Gray, N. S., Clemons, P. A., Silver, S., Wu, X., Zhao, W. N., Read-Button, W., Wu, X., Haggarty, S. J., Ronco, L. V., Boehm, J. S., Schreiber, S. L., Doench, J. G., Bittker, J. A., Root, D. E., Wong, B. and Golub, T. R. (2017) A Next Generation Connectivity Map: L1000 Platform and the First 1,000,000 Profiles. Cell 171, 1437-1452 e1417.


Copyright(c) Korean Endocrine Society. All rights reserved.